VIDEO:
PDF:
Descaragar PDF

MARCAPASOS
Las
células del nudo SA tienen un potencial de membrana de reposo de menos 65 mV.
Las células del nudo SA normalmente se despolarizan en forma espontánea por la
presencia de una corriente de marcapasos de despolarización diastólica (fase
4). Los conductos iónicos especializados que incrementan la corriente del
marcapaso no se muestran en esta animación. La corriente del marcapaso
despolarizan gradualmente las células en el nudo sinusal hasta que el potencial
de membrana alcanza el voltaje umbral necesario para desencadenar el potencial
de acción.
DESPOLARIZACIÓN
La fase
de de despolarización rápida inicial del potencial de acción en las células del
nudo sinusal se debe a los conductos de calcio (Ca2+) controlados por voltaje,
y la mayor parte de la corriente proviene de la entrada de Ca2+ a través de los
conductos de Ca2+ de tipo L. Tales conductos iónicos controlados por voltaje se
cierran en estado de reposo y se abren o "activan" cuando se alcanza
el voltaje umbral. Cuando estos conductos están "activos" permiten el
flujo de iones de Ca2+ hacia la célula. La entrada de Ca2+ a las células
desencadena la liberación adicional de Ca2+ del retículo sarcoplásmico (SR)
hacia la célula. Esto se conoce como liberación de calcio inducida por calcio
(CIRC) y ocurre a través de conductos específicos en la membrana del retículo
sarcoplásmico, conocidos como receptores de rianodina (RyR).
MESETA
Con el
tiempo, los conductos de Ca2+ de tipo L sufren un cambio conformacional a
estados de "inactividad", cerrados o sin conductancia, incluso aunque
el potencial de membrana celular permanezca mayor del voltaje umbral. Los
receptores de rianodina en el retículo sarcoplásmico también se cierran y, en
términos generales, se interrumpe la entrada de Ca2+ hacia el citoplasma. El
Ca2+ liberado en el citoplasma de las células del nudo sinusal se elimina del
citoplasma por acción de SERCA (ATPasa de calcio del retículo
sarco-endoplásmico), una bomba de Ca2+ que consume ATP que se encuentra en el
retículo sarcoplásmico y que bombea Ca2+ de nuevo hacia el retículo
sarcoplásmico y a través de un intercambiador de sodio-calcio que desplaza Ca2+
fuera de la célula en intercambio por Na+, que entra a la célula.
REPOLRIZACIÓN
Durante
la fase 3 del potencial de acción, las membranas de las células sinusales se
despolarizan por la salida de potasio (K+) fuera de la célula a través de la
activación de conductos de K+ controlados por voltaje. Los gradientes relativos
de sodio (Na+) y K+ y el gradiente eléctrico a través de la membrana celular
finalmente se restablece por la acción de la bomba de Na+- K+ -ATPasa y las
células sinusales nuevamente están listas para la despolarización espontánea.
RESUMEN
• La corriente
de marcapasos causa la despolarización gradual de la membrana celular.
• Los
conductos de Ca2+ de tipo L se abren cuando se alcanza el umbral de membrana.
• CIRC:
la entrada de Ca2+ induce a RyR para que libere Ca2+ del retículo
sarcoplásmico.
• Se
cierran los conductos de Ca2+ de tipo L y RyR.
• Se
elimina el Ca2+ del citoplasma por acción de SERCA y por intercambiadores de
Na+/Ca2+
• Se
abren los conductos de K+ controlados por voltaje y se despolariza la membrana
celular.
• Se
restablecen los gradientes de Na+ y K+ por acción de la bomba de Na+- K+
-ATPasa
• Una vez
más se inicia la corriente del marcapasos.
Antagonistas de los Conductos de Calcio
El
verapamilo y diltiazem son fármacos que reducen la frecuencia cardiaca en
ciertas formas de taquicardia supraventricular. Los antagonistas de los
conductos de calcio actúan al inhibir los conductos de Ca2+ de tipo L, con lo
que se incrementa el voltaje umbral necesario para la abertura de los conductos
y se reduce la cantidad de calcio que penetra a la célula. La mayor parte de la
corriente de despolarización hacia el interior de la célula que ocurre por la
despolarización de las células del nudo SA se debe a la entrada del ion calcio
a través de los conductos de Ca2+ de tipo L, y el efecto de estos fármacos
consiste en inhibir la automaticidad y reducir la frecuencia cardiaca. Con
concentraciones elevadas de estos fármacos, la entrada de Ca2+ puede inhibirse
lo suficiente, de forma que la despolarización de las células sinusales se
bloquea por completo (una condición conocida como asistolia) y otras células en
el corazón con automatismo intrínseco se pueden volver marcapasos y mantener la
frecuencia cardiaca, aunque a una frecuencia más baja que el ritmo sinusal
normal.
Acetilcolina
La
acetilcolina liberada del nervio vago reduce la frecuencia cardiaca al unirse a
receptores muscarínicos en la membrana de las células sinusales. La activación
de estos receptores incrementa la entrada de K+ a través de los conductos de K+
y reduce la despolarización durante la diástole, lo que inhibe la automaticidad
de las células sinusales.
Agonistas Adrenérgicos Beta
La
noradrenalina (NE) y adrenalina (Epi) que se liberan del sistema nervioso
simpático, incrementan la frecuencia cardiaca al activar los receptores adrenérgicos
beta en la membrana de las células sinusales. La activación de los receptores
adrenérgicos beta causa la activación de la adenililciclasa, que estimula la
producción de cAMP. El incremento en la producción intracelular de cAMP activa
la proteína cinasa A (PKA), una enzima que cataliza la incorporación de fosfato
en varias proteínas, lo que incluye las propias de los conductos de Ca2+ de
tipo L, RyR y fosfolambano (PL). El resultado es que entra más calcio a la
célula a través de los conductos de Ca2+ de tipo L, es bombeado hacia el
retículo sarcoplásmico por acción de SERCA y se libera del retículo
sarcoplásmico por RyR. El efecto de estos cambios en la manipulación del calcio
consiste en el incremento de la automaticidad de las células sinusales y la
capacidad de éstas para recuperarse después de la despolarización.
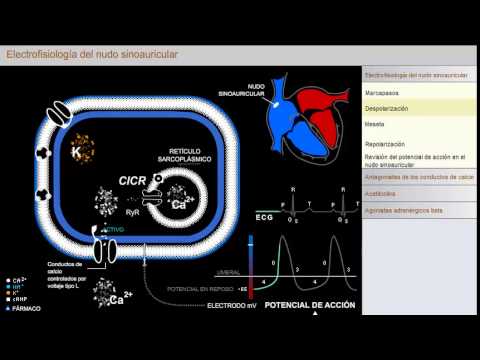 En esta animación se revisa la electrofisiología del nudo sinoauricular con especial atención a los conductos iónicos en el nudo sinusal que son el objetivo primario de los fármacos utilizados en el tratamiento de arritmias. Los iones se desplazan a través de las membranas celulares en respuesta a gradientes eléctricos y de concentración a través de conductos iónicos específicos, por medio de intercambiadores y por transportadores que bombean iones contra gradientes de concentración. El potencial de acción registrado en las células cardiacas refleja la suma de todos los desplazamientos iónicos a través de los diversos conductos iónicos, transportadores e intercambiadores. El nudo sinusal, también conocido como nudo sinoauricular (SA), es el conjunto de células que actúan como marcapaso natural del corazón. Dichas células se despolarizan de manera espontánea, una propiedad conocida como automaticidad. Los impulsos de despolarización generados en el nudo SA más tarde se propagan al resto del corazón. Como la tasa de despolarización espontánea, o automaticidad, es más rápida en las células del nudo sinusal, éste actúa como marcapasos natural del corazón.
En esta animación se revisa la electrofisiología del nudo sinoauricular con especial atención a los conductos iónicos en el nudo sinusal que son el objetivo primario de los fármacos utilizados en el tratamiento de arritmias. Los iones se desplazan a través de las membranas celulares en respuesta a gradientes eléctricos y de concentración a través de conductos iónicos específicos, por medio de intercambiadores y por transportadores que bombean iones contra gradientes de concentración. El potencial de acción registrado en las células cardiacas refleja la suma de todos los desplazamientos iónicos a través de los diversos conductos iónicos, transportadores e intercambiadores. El nudo sinusal, también conocido como nudo sinoauricular (SA), es el conjunto de células que actúan como marcapaso natural del corazón. Dichas células se despolarizan de manera espontánea, una propiedad conocida como automaticidad. Los impulsos de despolarización generados en el nudo SA más tarde se propagan al resto del corazón. Como la tasa de despolarización espontánea, o automaticidad, es más rápida en las células del nudo sinusal, éste actúa como marcapasos natural del corazón.
![LIBRO | Fisiopatologia - Porth 7ed [ESPAÑOL] [PDF] LIBRO | Fisiopatologia - Porth 7ed [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEimjbL6LT_Z6d7Eu0E1yC6b2onCRoZtDwVpjEt35wdoXJs9ILNxAsP5_XNCdl5TapQ9TnvReb_aEPQgj20IfvVx5CuNL0aZathiFRcaxP_9WETriXKmL6CgcaWhnZVA9ef6k0qJpaWKynMJ/s72-w482-c-h591-no/1.jpg)
![LIBRO | Fisiopatologia - Porth 9ed [ESPAÑOL] [PDF] LIBRO | Fisiopatologia - Porth 9ed [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEi79OPTpVDjhWmNUjxiGBU-hC2JxPmpdfNR0wdyv_ftkeZO1PBSMcjwwpHQcUHSRnNdjMmiIsnKgh4yYE-0BlNrtrAax3dRTS3baRrXnt_PjmsEBzFWnkhvUOK2wA6SJYRR1ppNYHTBV6s/s72-c/porth.jpg)
![LIBRO | Rumack - Diagnostico por Ecografia 3ra Ed Tomo 1 [ESPAÑOL] [PDF] LIBRO | Rumack - Diagnostico por Ecografia 3ra Ed Tomo 1 [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj7TL7kFXNMJSZA8cAH-gH3RSpii2LbH2Au25HyqjWdfId5D_kF-_RZIMZeSdJJGkYRKwY1vBab9vS0xnatB1rvXHJ2kBvaBk4e868EHWZ_xj9SMcaH5Nvo1lr7glUHYuv3HMmtmpWNy0lS/s72-w306-c-h400-no/1.jpg)
![LIBRO | Microbiologia Medica - Murray 7ma Ed [ESPAÑOL] [PDF] LIBRO | Microbiologia Medica - Murray 7ma Ed [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEisquvrRk6C-WfZIvx7QfTV-6WL0lqOuSBUJ589hpujlQi2rxQKdQzxDKZEJYqxzz4-Zug7lSQKw_BuhcuYK8KhIYD4V1k5PuDp1fe6T0mJdixY0snkxzHj8ahFMoTN3YyJC9j1yjee0_I/s72-c/Microbiologia.jpg)
![LIBRO | Goodman Gilman Las Bases Farmacológicas de la Terapéutica 12ed [ESPAÑOL] [PDF] LIBRO | Goodman Gilman Las Bases Farmacológicas de la Terapéutica 12ed [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEgUSn8akiMDV9L1ULfhk_ia031b25f9kF_BUy7_avmG16Y2QBGdHKC58Sms0MoNukK5SPnbFvS32LtxDfoxBDgaTC30vQTrXv7jvjUisAFjjXcH5Hm1Vv_AKrIZEBB9naUpfW1v-I2KosFz/s72-w455-c-h591-no/goodman.jpg)
![LIBRO | Dermatología - Fitzpatrick 7ed (Tomo 1) [ESPAÑOL] [PDF] LIBRO | Dermatología - Fitzpatrick 7ed (Tomo 1) [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEh_wYW6m9TkrkJ5XuFxXHMMm-_K1pEBgv_vqj3xatUwX4zLsFEnS3SzonOCyNZQrSzczFZQgiw34soMf6vd_wog1wBXqVOHSuWLyDQwxtq5UXZeMKfkCgpjwJdIjz76IHXVqBUSksFzW7Q/s72-c/Fitzpatrick.jpg)

![LIBRO | Neurología - Zarranz 5ed [ESPAÑOL] [PDF] LIBRO | Neurología - Zarranz 5ed [ESPAÑOL] [PDF]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhkDSsoVvCseluT7N7anR_h1DK58lNVtVx5Vklbocu77zECw49tjocrQ-F8eKq6xjRbWE-JEaOTd5APklmRHSFK0s2QFT_I6r8P6MnXzCmcW0RSPkjrm1FyCtYGjeocDfFCDIi5OLdm1WXJ/s72-c/ZARRANZ.jpg)
